به گزارش ایمنا ۱۸ اردیبهشت مصادف با 8 می هر سال به نام روز جهانی تالاسمی نامگذاری شده است. هدف از نامگذاری این روز، توجه بیشتر مسئولین و مردم به بیماری تالاسمی است. همچنین فراهم آمدن امکانات درمانی مطابق با استاندارد های جهانی و دستیابی به خون سالم و کافی برای همه بیماران تالاسمی و عدم تولد بیمار تالاسمی درکشوراهداف عمده ای است که همه افراد و سازمان های درگیر در این بیماری به آنها می اندیشند و برای دستیابی به آن تلاش می کنند.
در بیماری تالاسمی هموگلوبین معیوب قادر به اکسیژن رسانی مطلوب به اعضا بدن نیست. بنابراین در این بیماری کمبود کلی هموگلوبین وجود ندارد، بلکه هموگلوبین غیرطبیعی افزایش یافته است.
هموگلوبین جزء انتقال دهنده اکسیژن در سلول های قرمز خونی است که شامل دو پروتئین به نام های آلفا و بتا است. اگر بدن توانایی تولید کافی از هر نوع پروتئین را نداشته باشد، سلول های خونی به طور کامل شکل نمیگیرند و توانایی انتقال اکسیژن کافی را ندارند.
در نتیجه تالاسمی یک نوع کم خونی است که در طفولیت آغاز میشود و تا پایان عمر به طول میانجامد. هر چند تالاسمی یک اختلال منفرد نیست، اما یک گروه اختلالات از طرق مشابه بدن انسان را درگیر میکند.
تالاسمی آلفا
افرادی که در آنها هموگلوبین به میزان کافی پروتئین آلفا تولید نمیکند به تالاسمی آلفا مبتلا میشوند. تالاسمی آلفا به طور شایع در آفریقا، خاورمیانه، هند، آسیای جنوبی، جنوب چین و نواحی مدیترانه یافت میشود. ۴ گونه تالاسمی آلفا وجود دارد که با توجه به آثار آنها بر بدن از خفیف تا شدید تقسیمبندی میشود.
در مرحله "حامل خاموش"، عموما فرد سالم است، زیرا کمبود بسیار کم پروتئین آلفا بر عملکرد هموگلوبین تأثیر نمیگذارد. اما به علت تشخیص مشکل، این مرحله حامل خاموش نامیده میشود. یک فرم غیر معمول از مرحله حامل خاموش که به واسطه جهش در هموگلوبین آلفا رخ میدهد، " هموگلوبین "کنستانت اسپرینگ" نام دارد. علت این این نامگذاری آن است که این موضوع در منطقهای در جامائیکا به نام کنستانت اسپرینگ کشف شده است.
در مرحله تالاسمی "آلفا خفیف" کمبود پروتئین آلفا بیشتر است. بیماران در این مرحله سلولهای قرمز خونی کمتر و کوچکتری دارند، اگر چه بسیار از بیماران علائمیاز بیماری را تجربه نمیکنند. پزشکان اغلب تالاسمی آلفا خفیف را با کم خونی فقر آهن اشتباه میگیرند و برای بیماران آهن تجویز میکنند. آهن هیچ تأثیری بر درمان کم خونی تالاسمی آلفا ندارد.
در بیماری هموگلوبین H، کمبود پروتئین آلفا به حدی است که منجر به کم خونی شدید و بروز مشکلاتی نظیر طحال بزرگ، تغییرات استخوانی و خستگی میشود. نامگذاری به علت هموگلوبین H غیرطبیعی است که سلولهای قرمز خون را تخریب میکند.
در بیماری "هیدروپس جنینی" یا تالاسمی "آلفای بزرگ"، در بررسی DNA فرد ژنهای آلفا مشاهده نمیشود. این در حالی است که بسیاری از این بیماران قبل یا در فاصله کوتاهی بعد از تولد میمیرند. در موارد بسیار نادری که بیماری قبل از تولد تشخیص داده میشود، تزریق خون داخل رحمی منجر به تولد کودکی با هیدروپس جنینی میشود. اما این نوزاد در سراسر زندگی خود به تزریق خون و مراقبتهای پزشکی نیازمند است.
تالاسمی بتا
این بیماری در افرادی که هموگلوبین، پروتئین بتا به اندازه کافی تولید نمیکند ایجاد میشود. تالاسمی بتا در مردم نواحی مدیترانه نظیر یونان و ایتالیا، ایران، شبه جزیره عربستان، آفریقا، جنوب آسیا و جنوب چین یافت میشود.
سه گونه تالاسمی بتا وجود دارد که با توجه به آثار آنها در بدن از خفیف تا شدید تقسیمبندی میشوند.
تالاسمی مینور
در این حالت کمبود پروتئین به حدی نیست که باعث اختلال در عملکرد هموگلوبین شود. یک فرد با این بیماری حامل صفت ژنتیکی تالاسمی است. این فرد به جز یک کم خونی خفیف در برخی موارد، مشکل دیگری را تجربه نخواهد کرد. همانند تالاسمی آلفای خفیف، گاهی ممکن است پزشک بخواهد فرد مبتلا به تالاسمی بتای مینور را به عنوان علامتی از کم خونی فقر آهن با تجویز نادرست مکمل آهن درمان کند.
تالاسمی بینابینی
در این حالت کمبود پروتئین بتا در هموگلوبین به اندازهای است که منجر به کم خونی نسبتا شدید و اختلالات قابل ملاحظهای در سلامت فرد نظیر بدفرمیهای استخوانی و بزرگی طحال میشود. در این مرحله طیف وسیعی از علائم وجود دارد. تفاوت کم بین علائم تالاسمی بینابینی و فرم شدیدتر (تالاسمی ماژور) میتواند گیج کننده باشد. بیماران مبتلا به تالاسمی بینابینی برای بهبود کیفیت زندگی و نه برای نجات یافتن، به تزریق خون نیازمند هستند.
تالاسمی ماژور
این مرحله شدیرترین فرم تالاسمی بتا است که کمبود شدید پروتئین بتا در هموگلوبین منجر به یک کم خونی تهدید کننده حیات میشود و فرد به انتقال خون منظم و مراقبتهای طبی فراوانی نیازمند است.
انتقال خون مکرر در طول عمر این بیماران منجر به تجمع بیش از حد آهن میشود که باید توسط تجویز عوامل کمک کننده در دفع، جهت جلوگیری از مرگ و نارسایی ارگانها درمان شوند.
انتقال خون؛ شایع ترین روش درمان تالاسمی
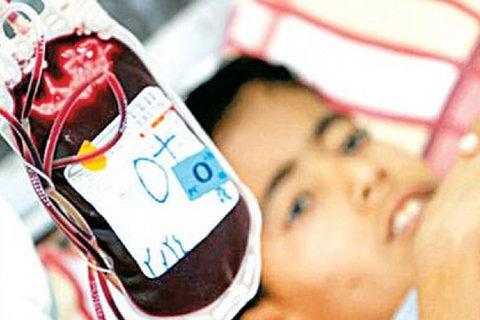
شایعترین درمان برای تمامیاشکال تالاسمی تزریق سلولهای قرمز خونی است. این تزریق خون برای فراهم آوردن مقادیری از سلولهای قرمز خونی سالم و هموگلوبین طبیعی که قادر به انتقال اکسیژن باشد، ضروری است.
در صورتی که بیمار تالاسمیک در گذشته به اندازه کافی خون دریافت نکرده باشد، لازم است جهت بهبود کیفیت زندگی وی، دفعات تزریق خون افزایش یابد. امروزه بسیاری از بیماران تالاسمی ماژور در هر دو یا سه هفته خون دریافت میکنند که معادل ۵۲ پاینت خون در یک سال و برابر ۴۷۳ میلیلیتر است.
افزایش بیش از حد آهن، مهم ترین علت مرگ بیماران تالاسمی ماژور
در بدن راه طبیعی جهت حذف آهن وجود ندارد، بنابراین آهن موجود در خون تزریق شده در بدن انباشته و وضعیتی را به نام "افزایش غیرطبیعی آهن" (Iron Overload) ایجاد میکند. آهن مازاد برای بافتها و ارگانهای بدن به ویژه قلب و کبد سمیاست و منجر به مرگ زودرس و یا نارسایی ارگانها در فرد بیمار میشود. اضافه بار آهن به ویژه در قلب، مهمترین علت مرگ و میر بیماران تالاسمی ماژور میباشد.
دفع آهن اضافی به کمک داروی " دسفرال"
برای کمک به دفع آهن اضافی، بیمار تحت درمان سخت و دردناک با دارویی به نام دسفرال (Desferal) قرار میگیرد. دارو از طریق یک سوزن متصل به پمپ و زیر پوست ناحیه معده یا پاها تزریق میشود.
تزریق این دارو پنج تا هفت بار در هفته و هر بار ۱۲ ساعت به طول میانجامد. دسفرال از طریق فرایندی به نام Chelation به آهن متصل میشود و با دفع آهن متصل به دسفرال میزان آهن ذخیره در بدن کاهش مییابد.
پیشگیری از بیماری تالاسمی
در حال حاضر موثرترین راه پیشگیری از بیماری تالاسمی، غربالگری این بیماری در سطح جمعیتی و سپس بررسی ملکولی افرادی است که در غربالگری در زمره افراد تحت خطر طبقهبندی شدهاند. برای این منظور در ایران برنامه کشوری غربالگری تالاسمی توسط وزرات بهداشت در حال انجام است.
مشاوره ژنتیک
مشاوره ژنتیک در افرادی که در غربالگری در زمره افراد تحت خطر طبقهبندی شدهاند و یا افرادی که دارای بستگان نزدیک مبتلا به تالاسمی هستند توصیه میشود. ریسک تکرار این بیماری در فرزندان بعدی یک زوج دارای فرزند مبتلا ۲۵٪ است که در صورت تعیین جهش در فرزند مبتلا و تایید ناقل بودن والدین میتوان با تشخیص قبل از تولد در طی دوران بارداری از وضعیت ابتلا یا عدم ابتلای جنین اطمینان حاصل کرد.






نظر شما